Проблема множественной лекарственной устойчивости (МЛУ) у патогенных микроорганизмов перешла в стадию глобального кризиса. Каждый год миллионы людей по всему миру сталкиваются с инфекциями, которые все труднее поддаются лечению. По данным ВОЗ, к 2050 году антибиотикорезистентные инфекции могут стать причиной 10 миллионов смертей ежегодно. В этом контексте открытие нового класса антибиотиков Novltex, разработанного международной группой ученых, приобретает особую значимость. Эти соединения демонстрируют высокую эффективность против патогенов со множественной устойчивостью, включая приоритетные для ВОЗ штаммы.
От Novo29 к рациональному дизайну
Исследователи взяли за основу недавно открытый класс антибиотиков Novo29 (клофибактин), выделенный из β-протеобактерий. Этот макроциклический пептид проявил впечатляющую антимикробную активность благодаря уникальному механизму действия – одновременному связыванию с несколькими предшественниками пептидогликана (C55-PP, Lipid II и Lipid III). Эти мишени консервативны у бактерий, но отсутствуют в клетках млекопитающих, что обеспечивает высокую селективность действия.
Однако есть существенный недостаток – синтез Novo29 обладает крайне низким выходом (около 1%). Вдобавок, ключевой компонент синтеза (D-гидроксиаспарагин, D-Hyn5) чрезвычайно дорог и отсутствует в коммерческом доступе. Ученые пошли по пути рационального дизайна, объединив макроциклическую структуру Leu10-тейксобактина (где вместо сложного D-Hyn5 используется доступный треонин) с N-концевым фрагментом Novo29. Так появился новый класс соединений – Novltex.
Однако есть существенный недостаток – синтез Novo29 обладает крайне низким выходом (около 1%). Вдобавок, ключевой компонент синтеза (D-гидроксиаспарагин, D-Hyn5) чрезвычайно дорог и отсутствует в коммерческом доступе. Ученые пошли по пути рационального дизайна, объединив макроциклическую структуру Leu10-тейксобактина (где вместо сложного D-Hyn5 используется доступный треонин) с N-концевым фрагментом Novo29. Так появился новый класс соединений – Novltex.
Технологический прорыв
Ключевым достижением стало создание эффективной методологии синтеза. Исследователи разработали платформу на основе твердофазного пептидного синтеза (SPPS) с использованием микроволнового связывания. Эта технология позволила заменить дефицитный D-Hyn5 на коммерчески доступный треонин, одновременно увеличив выход целевого продукта с 1% до впечатляющих 25-30%. Время циклов связывания сократилось до 10 минут, что делает процесс экономически выгодным и пригодным для масштабирования.
Для систематической оптимизации структуры ученые синтезировали библиотеку из 16 аналогов Novltex. Первые десять соединений были направлены на изучение влияния стереохимии макроцикла и N-концевого фрагмента. Аналог 4 (с D-конфигурацией Leu2) показал многообещающую активность против MRSA (минимальная ингибирующая концентарция (МИК) 2-4 мкг/мл), сопоставимую с ванкомицином. Это подтвердило гипотезу о критической важности пространственной ориентации гидрофобных остатков (Phe1 и Leu2) для эффективного взаимодействия с бактериальной мембраной.
Для систематической оптимизации структуры ученые синтезировали библиотеку из 16 аналогов Novltex. Первые десять соединений были направлены на изучение влияния стереохимии макроцикла и N-концевого фрагмента. Аналог 4 (с D-конфигурацией Leu2) показал многообещающую активность против MRSA (минимальная ингибирующая концентарция (МИК) 2-4 мкг/мл), сопоставимую с ванкомицином. Это подтвердило гипотезу о критической важности пространственной ориентации гидрофобных остатков (Phe1 и Leu2) для эффективного взаимодействия с бактериальной мембраной.
Высшая точка оптимизации
Следующий этап оптимизации был посвящен модификации позиции Leu2. Гипотеза о том, что увеличение гидрофобности боковой цепи может усилить мембранное взаимодействие, привела к синтезу серии аналогов 11-16, где Leu2 заменялся на аминокислоты с циклическими гидрофобными остатками. Аналог 12 (Leu2Cha-Novltex), содержащий циклогексилаланин в позиции 2, продемонстрировал феноменальную активность с МИК всего 0,25 мкг/мл против MRSA – в 32 раза превосходя предшественника с более короткой боковой цепью.
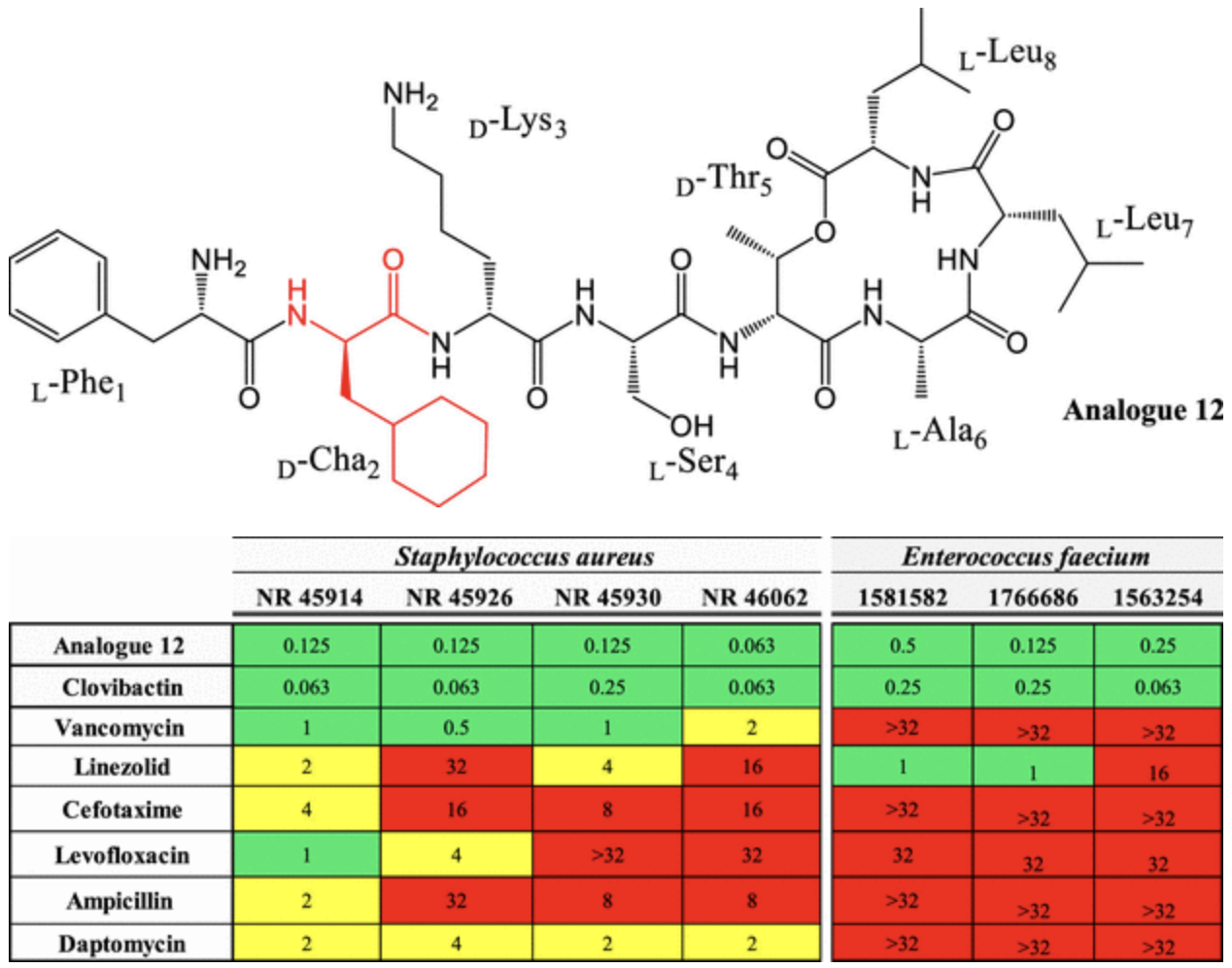
Тестирование Аналога 12 против клинических штаммов МЛУ-патогенов, включая ванкомицин-резистентный Enterococcus faecium, показало МИК в диапазоне 0,063-0,5 мкг/мл. Особенно впечатляет его способность значительно сокращать бактериальную популяцию всего за 6 часов, тогда как ванкомицину для достижения аналогичного эффекта требуется вчетверо больше времени при более высоких дозах. Примечательно, что при длительном воздействии Аналога 12 у бактерий не формировалось устойчивых мутантов – серьезное преимущество в борьбе с резистентностью.
Механизм действия и безопасность
Молекулярные исследования подтвердили, что Novltex сохраняет основной механизм действия исходного соединения – целенаправленное связывание с Lipid II, ключевым компонентом бактериальной стенки. Дополнительные исследования выявили, что Аналог 12 также вызывает деполяризацию цитоплазматической мембраны у MRSA, что объясняет его мощное бактерицидное действие.
Профиль безопасности Аналога 12 оказался обнадеживающим. В исследованиях in vitro на различных типах человеческих клеток не было выявлено токсического эффекта даже при концентрациях, значительно превышающих терапевтические дозы. Низкая гемолитическая активность делает соединение потенциально пригодным для инъекционного введения.
Профиль безопасности Аналога 12 оказался обнадеживающим. В исследованиях in vitro на различных типах человеческих клеток не было выявлено токсического эффекта даже при концентрациях, значительно превышающих терапевтические дозы. Низкая гемолитическая активность делает соединение потенциально пригодным для инъекционного введения.
Перспективы применения
Использование коммерчески доступных компонентов и высокий выход продукта решают ключевую проблему масштабирования, с которой сталкиваются многие перспективные соединения. Сочетание высокой эффективности против МЛУ-патогенов, отсутствия формирования резистентности и благоприятного профиля безопасности делает этот класс соединений крайне перспективным для дальнейшей разработки.
Если клинические испытания подтвердят лабораторные данные, Novltex может стать важным инструментом в арсенале врачей, борющихся с инфекциями, не поддающимися традиционной терапии. В условиях, когда новые антибиотики появляются крайне редко, этот прорыв может спасти миллионы жизней и изменить подход к борьбе с антибиотикорезистентностью.
Если клинические испытания подтвердят лабораторные данные, Novltex может стать важным инструментом в арсенале врачей, борющихся с инфекциями, не поддающимися традиционной терапии. В условиях, когда новые антибиотики появляются крайне редко, этот прорыв может спасти миллионы жизней и изменить подход к борьбе с антибиотикорезистентностью.
Дата публикации: 2025.10.07
Первоисточник:
Malkawi E. et al. Novltex: A New Class of Antibiotics with Potent Activity against Multidrug-Resistant Bacterial Pathogens─Design, Synthesis, and Biological Evaluation. J Med Chem. 2025 Sep 25;68(18):19143-19152. doi: 10.1021/acs.jmedchem.5c01193. Epub 2025 Sep 16. PMID: 40957081; PMCID: PMC12481569.
https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c01193
Malkawi E. et al. Novltex: A New Class of Antibiotics with Potent Activity against Multidrug-Resistant Bacterial Pathogens─Design, Synthesis, and Biological Evaluation. J Med Chem. 2025 Sep 25;68(18):19143-19152. doi: 10.1021/acs.jmedchem.5c01193. Epub 2025 Sep 16. PMID: 40957081; PMCID: PMC12481569.
https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c01193
